Биологи проектируют новые ферменты
|
Ученые из Калифорнийского университета в Беркли изготовили семь новых ферментов (четыре из которых не имеют природных аналогов) путем замены нескольких ключевых аминокислот в активном центре белка гамма-гумулен синтазы, участвующего в образовании смолы у пихты. Новые ферменты осуществляют синтез различных терпенов — веществ, используемых в фармакологии, пищевой и химической промышленности. Исследование показало, что для возникновения нового фермента в ходе эволюции порой бывает достаточно очень небольшого числа мутаций.
Молекулы ферментов (белков, катализирующих разнообразные биохимические реакции) состоят из сотен аминокислот, однако не все они одинаково важны. Многие аминокислоты можно заменить другими без заметного изменения свойств фермента. Ключевую роль играют аминокислоты, составляющие активный центр фермента — тот сравнительно небольшой участок белковой молекулы, который связывает молекулу субстрата и осуществляет с ней необходимые манипуляции, превращая в конечный продукт. Замена всего одной-двух аминокислот в активном центре может привести к радикальному изменению свойств фермента. В большинстве случаев, конечно, фермент от этого просто-напросто «портится», снижает производительность или вовсе становится нефункциональным. В других случаях это может привести к модификации или даже полной смене функции, то есть к появлению нового фермента.
Биологи давно поняли, что такое точечное мутирование, затрагивающее активные центры ферментов, является распространенным и весьма эффективным способом молекулярной эволюции (именно так, например, бактерии очень быстро вырабатывают устойчивость к новым антибиотикам; см. Пути эволюции предопределены на молекулярном уровне, Элементы, 12.04.2006). Однако одно дело — понять общий принцип, и совсем другое — получить экспериментальные подтверждения и научиться использовать на практике.
В последние годы многие исследователи занялись поиском способов целенаправленного изменения свойств ферментов. Подобные технологии очень важны для фармакологии и химической промышленности, поскольку ферменты — чрезвычайно эффективные катализаторы, способные в тысячи раз ускорить синтез чуть ли не любых химических соединений.
Задача усложняется отсутствием эффективной универсальной методики предсказания свойств фермента на основе его аминокислотной последовательности. Поэтому действовать обычно приходится методом тыка — заменять отдельные аминокислоты и смотреть, что получилось. Заметив отклонение свойств белка в желаемую сторону, удачных мутантов отбирают и снова подвергают мутированию. Таким образом, по сути дела, имитируется природный эволюционный процесс, основанный на случайных мутациях и отборе. Эта методика результативна, но очень трудоемка. Поэтому очень важно найти способы оптимизации случайного поиска, чтобы сократить число перебираемых вариантов.
|
В последнем номере журнала Nature опубликована статья американских исследователей, которым удалось добиться значительных успехов в этом направлении. Ученые экспериментировали с ферментом, принимающим участие в образовании смолы у американской пихты Abies grandis — гамма-гумулен синтазой (gamma-humulene synthase). Этот фермент, состоящий из 593 аминокислот, относится к числу «неразборчивых», или неспецифических, поскольку он синтезирует из одного и того же субстрата (фарнезил-дифосфата) не какое-то одно конкретное вещество, а смесь из 52 различных веществ — сесквитерпенов. Преобладает в этой смеси гамма-гумулен (вещество, вынесенное в название фермента), однако его доля составляет лишь 45,1% от общей массы продуктов реакции. По-видимому, пихту вполне устраивает такой «винегрет», добавляемый в смолу, однако фармакологи и химики предпочли бы иметь в своем распоряжении более специфические катализаторы для синтеза конкретных терпенов, которые используются как ароматизаторы, сырье для производства лекарств и пищевых добавок и т. д.
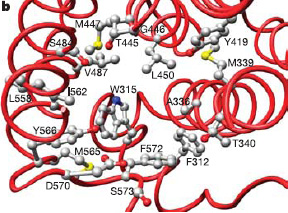
Исследователи начали с построения трехмерной модели молекулы гамма-гумулен синтазы (реконструкция трехмерной структуры белков — это целая отдельная наука, в которой в последние годы достигнуты большие успехи). Имея трехмерную модель, можно определить, где находится активный центр и какие аминокислоты в него входят. Затем из общего числа аминокислот активного центра были исключены те, которые составляют так называемый «консервативный мотив» — эти аминокислоты одинаковы у всех известных терпен-синтаз, из чего можно сделать вывод, что они нужны для синтеза любых терпенов, и изменение каждой из них, скорее всего, приведет к общему снижению производительности фермента.
В результате осталось 19 аминокислот, входящих в активный центр и не входящих в консервативный мотив, с которыми и начали экспериментировать. Ученые исходили из предположения, что именно среди этих аминокислот скорее всего отыщутся те, от которых зависит состав производимой ферментом смеси продуктов.
Даже для 19 аминокислот перебрать все возможные мутации и их комбинации — задача неподъемная (1920, или примерно 5 ? 1024 комбинаций), поэтому ученым пришлось сделать еще одно допущение. Они решили пренебречь взаимным влиянием мутаций друг на друга и исходить из предположения, что все мутации аддитивны, то есть каждая конкретная мутация меняет функциональность фермента строго определенным образом, независимо от того, какие мутации он претерпел до этого. В данном случае такой подход в целом оправдался, хотя известно, что в других случаях суммарный эффект нескольких мутаций может быть вовсе не похож на простую сумму эффектов этих мутаций, взятых по отдельности.
Ученые исследовали эффекты, производимые заменой каждой из 19 аминокислот по отдельности (для каждой аминокислоты возможно 19 различных замен, так что пришлось перебрать всего 361 вариант). Затем, исходя из допущения об аддитивности эффектов отдельных мутаций, оптимальные сочетания мутаций были вычислены уже чисто теоретически, при помощи несложных формул. Наконец, эти теоретически предсказанные комбинации были синтезированы и испытаны в пробирке. В некоторых случаях теоретические ожидания не оправдались (в основном из-за того, что не сработало допущение об аддитивности), но в итоге ученым все-таки удалось получить целых семь новых ферментов, пригодных для производства отдельных сесквитерпенов. Четыре из них не имеют природных аналогов, в том числе сибирен синтаза (производит 78,1% сибирена, тогда как исходная гамма-гумулен синтаза производит лишь 23,1% этого сесквитерпена) и альфа-лонгипинен синтаза (дает 61,5% альфа-лонгипинена против исходных 4,7%). Были получены и две новых гамма-гумулен синтазы, производящих заметно больше гамма-гумулена, чем исходный фермент (54,6% и 85,7% против исходных 45,1%).
Все новые ферменты отличаются от исходного очень небольшим количеством аминокислотных замен (от 1 до 5). Это подтвердило имеющиеся представления о том, что небольшое число мутаций в активном центре может привести к радикальной смене функции фермента. Две новые гамма-гумулен синтазы несут разные наборы мутаций и представляют собой пример «параллельной эволюции», приведшей к одной и той же цели разными путями (как и в случае с независимым появлением пятен на крыльях у разных видов дрозофил, о чем «Элементы» недавно писали).
По-видимому, в ближайшие годы технологии искусственного изготовления новых ферментов будут быстро развиваться. Авторы полагают, что очень скоро можно будет спроектировать даже ферменты для производства веществ, не встречающиеся в живой природе.
Источник: Yasuo Yoshikuni, Thomas E. Ferrin, Jay D. Keasling. Designed divergent evolution of enzyme function // Nature. 2006. V. 440. P. 1078-1082.
Александр Марков